[화이트페이퍼=김새봄 기자] GC녹십자가 개발 중인 코로나19 혈장치료제 ‘GC5131A’가 환자를 대상으로 하는 임상시험에 돌입한다.
GC녹십자는 “식품의약품안전처로부터 코로나19 혈장치료제 ‘GC5131A’의 임상 2상을 승인받았다”고 20일 밝혔다. 다른 치료제로 허가받은 약을 활용하는 약물 재창출 연구 이외에 개발 중인 코로나 치료제 중 임상 2상을 승인받은 것은 이번이 처음이다.
임상 1상은 건강한 사람을 대상으로 안전성을 확인하고, 임상 2상은 소규모 환자를 대상으로 안전성과 약의 효능을 확인한다.
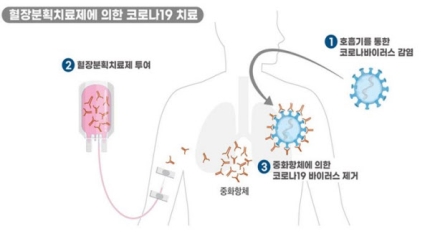
혈장치료제는 코로나 회복 환자의 혈장(혈액의 액체 성분)에서 코로나 바이러스에 대항할 수 있는 면역 항체들을 분리해 고농도로 농축한 의약품이다. 혈장치료제는 신종 감염병 발발 시 가장 빠르게 투약 가능한 의약품으로 분류된다. 혈장치료제와 달리 ‘항체치료제’는 바이러스와 잘 결합하는 항체를 골라내 외부에서 세포 배양으로 대량 생산한다.
‘GC5131A’는 코로나19 완치자의 혈장에서 다양한 항체가 들어있는 면역 단백질을 분리해 만든 치료제다. GC녹십자는 폐렴 환자와 고령, 기저질환이 있는 고위험군 환자 60명을 대상으로 임상을 진행한다. 임상은 삼성서울병원, 서울아산병원, 중앙대병원, 고대안산병원, 충남대병원, 연대 세브란스병원 등 총 6개 병원에서 진행될 계획이다. 회사 측은 이미 임상시험용 제제 생산이 완료된 만큼, 가까운 시일 내 환자 투여가 개시될 것이라고 설명했다.
식약처에 따르면 현재 국내 코로나 치료제 및 백신 임상 시험은 총 16건이 진행되고 있다. 치료제가 14건이고 백신이 2건이다.
한편, GC녹십자는 이와 별도로 ‘코로나19 혈장치료제 개발 얼라이언스(CoVlg-19 Plasma Alliance)’에 합류해 다케다(Takeda), CSL Behring 등 글로벌 혈액제제 기업들과 해외용 혈장치료제 개발에도 참여하고 있다.


